Авторы: Амеркулова Н.О., врач неонатолог ГКП на ПВХ «Городская многопрофильная больница г. Конаев»
Турленбаева А.А. врач неонатолог ГКП на ПВХ «Городская многопрофильная больница г. Конаев»
Аннотация. Геморрагическая болезнь новорождённых (ГБН) — патологическое состояние, обусловленное дефицитом витамина K, проявляющееся повышенной кровоточивостью и высоким риском тяжёлых осложнений. В статье рассмотрены современные подходы к профилактике, диагностике и лечению ГБН. Особое внимание уделено парентеральному введению витамина K как эффективной стратегии профилактики. Представлены данные эпидемиологии, классификации, а также методы лечения, включая минимально инвазивные хирургические вмешательства. Авторы подчёркивают необходимость унификации протоколов профилактики и дальнейших исследований для улучшения исходов у новорождённых.
Ключевые слова: геморрагическая болезнь новорождённых, витамин K, диагностика, профилактика, неонатология, лечение
Геморрагическая болезнь новорожденных (ГБН) представляет собой актуальную проблему современной педиатрии и неонатологии. Особую важность приобретает своевременная диагностика и профилактика, позволяющие предотвращать серьёзные осложнения и улучшать исходы для здоровья новорождённых. Современный этап развития медицины требует применения эффективных методов профилактики, диагностики и лечения ГБН, а также учета факторов риска, связанных с состоянием матери и особенностями новорождённого, для обеспечения комплексного подхода к этой проблеме.
Геморрагическая болезнь новорожденных (ГБН) является патологическим состоянием, характеризующимся повышенной кровоточивостью у новорожденных вследствие дефицита витамина К, который играет ключевую роль в синтезе факторов свертывания крови. Отсутствие своевременной профилактики ГБН может привести к серьезным кровотечениям, включая внутричерепные, что представляет угрозу для жизни младенца.
Геморрагическая болезнь новорожденных (ГБН) характеризуется разнообразной распространённостью, которая не зависит от пола и расы ребёнка, но варьируется в зависимости от региона и наличия профилактических мер. В таблице 1 представлена эпидемиология ГБН.
Таблица 1 — Эпидемиология геморрагической болезни новорожденных (ГБН)
| Регион | Общая заболеваемость (на 100 тыс.) | Поздняя форма ГБН (на 100 тыс.) |
| Россия | 0,25–1,7% | 4,4–7,2 |
| США | 250–1700 (при отсутствии профилактики) | — |
| Австралия | 0,84 | 0,61 |
| Швейцария | — | 0,87 |
| Нидерланды | — | 1,8 |
| Канада | ~1 (на 140–170 тыс. новорожденных) | — |
| Непал | 5–80 (при отсутствии профилактики) | — |
В России частота ГБН составляет от 0,25% до 1,7% среди всех новорожденных. В США при отказе от профилактики заболеваемость достигает 250–1700 случаев на 100 тысяч новорожденных. В Австралии этот показатель составляет 0,84 на 100 тысяч живорождённых, что свидетельствует о более низкой заболеваемости при эффективной профилактике [3].
Поздняя форма ГБН встречается реже. В России её частота составляет от 4,4 до 7,2 случая на 100 тысяч новорожденных. В зарубежных странах показатели несколько ниже: в Швейцарии – 0,87, в Нидерландах – 1,8, в Австралии – 0,61 на 100 тысяч живорождённых. В Канаде благодаря широкому применению профилактических мер, включая введение витамина К, заболеваемость составляет примерно 1 случай на 140–170 тысяч новорожденных. В Непале, где профилактика отсутствует, заболеваемость значительно выше – от 5 до 80 случаев на 100 тысяч новорожденных [4].
Особое внимание уделяется факторам риска, повышающим вероятность развития ГрБН. Среди них можно выделить отсутствие профилактического введения витамина К после рождения, исключительно грудное вскармливание (грудное молоко содержит значительно меньшие концентрации витамина К по сравнению с адаптированными смесями), а также наличие сопутствующих заболеваний, влияющих на всасывание или метаболизм витамина К, таких как холестаз и синдром мальабсорбции (Shearer, 2009).
Таким образом, многочисленные исследования убедительно доказывают необходимость и эффективность профилактических мер, направленных на предотвращение геморрагической болезни новорожденных, включая рутинное введение витамина К. Эти меры рекомендованы Всемирной организацией здравоохранения (ВОЗ) и многими национальными педиатрическими ассоциациями для снижения младенческой смертности и заболеваемости.
Новорожденные испытывают дефицит витамина K по нескольким причинам: ограниченный транспорт витамина через плаценту, низкое содержание витамина в грудном молоке и недостаток кишечной микрофлоры, которая синтезирует витамин K2 [1]. Этот дефицит приводит к снижению активности факторов свертывания, удлинению протромбинового времени и накоплению некарбоксилированных белков, таких как PIVKA-II (дескарбоксипротромбин) [2].
Согласно этиологии, геморрагическая болезнь новорожденных (ГБН) делится на первичную и вторичную формы.
Первичная ГБН развивается преимущественно у детей на исключительно грудном вскармливании при отсутствии профилактики витамином K [2].
Вторичная ГБН обусловлена дополнительными факторами риска. Со стороны матери это может быть приём во время беременности непрямых антикоагулянтов, противосудорожных препаратов, антибиотиков широкого спектра действия, а также наличие гестоза, преэклампсии или фетоплацентарной недостаточности [3]. У ребёнка вторичная ГБН часто связана с такими заболеваниями, как синдром мальабсорбции, муковисцидоз, целиакия, атрезия желчевыводящих путей, холестаз или кистофиброз поджелудочной железы [4].
Таким образом, понимание патогенеза и факторов риска ГБН является основой для разработки эффективных профилактических и терапевтических стратегий.
Клиническая классификация, предложенная Международным обществом по тромбозу и гемостазу в 1999 году, делит ГБН на три формы в зависимости от возраста дебюта, которые представлены на рисунке 1.
Клинические проявления ГБН зависят от её формы и степени тяжести, которые можно классифицировать на кожные и слизистые проявления, поражение желудочно-кишечного тракта, внутренние кровотечения, поражение центральной нервной системы и повреждения опорно-двигательной системы.
Кожные и слизистые проявления ГБН нередко проявляется кровотечениями из пупочной культи, множественными петехиями и экхимозами на коже и слизистых оболочках. Возможны «подтекания» из мест инъекций, а у мальчиков — кровотечения после обрезания [5].
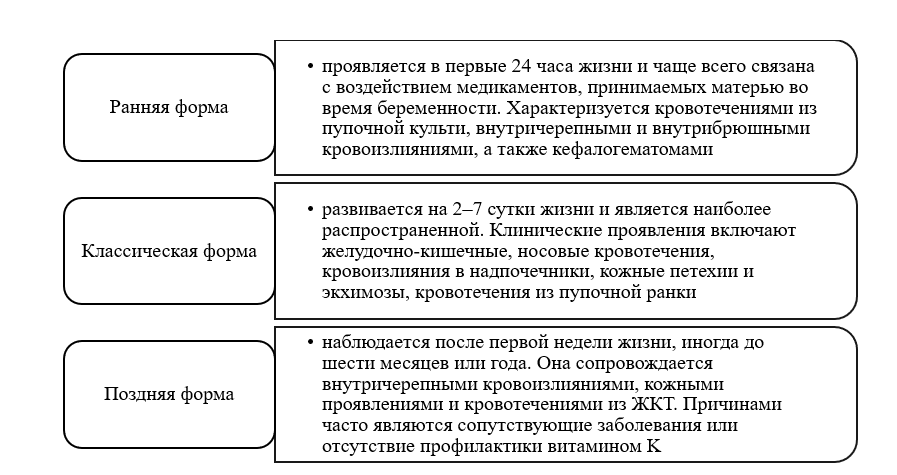
Рисунок 1 – Формы ГБН
Симптоматика поражение желудочно-кишечного тракта включает рвоту с примесью крови («кофейная гуща»), мелену (черный дегтеобразный стул), а также эрозии слизистой оболочки желудка и двенадцатиперстной кишки. При массивных кровотечениях развивается гипербилирубинемия вследствие гемолиза эритроцитов [5].
Внутренние кровотечения часто поражаются паренхиматозные органы, такие как печень, селезенка и надпочечники. Легочные кровотечения могут потребовать респираторной поддержки, что является прогностически неблагоприятным фактором [3].
Наиболее серьёзным осложнением ГБН является внутричерепное кровоизлияние, которое может проявляться вялостью, выбуханием родничков, судорогами, изменением сознания. Такие кровоизлияния включают субарахноидальные, субдуральные и внутрижелудочковые формы. Они часто приводят к развитию постгеморрагической гидроцефалии, центральных параличей и психоневрологических нарушений [7].
Дефицит витамина K снижает выработку остеокальцина, что увеличивает риск переломов трубчатых костей, особенно у детей с поздней формой ГБН.
ГБН, особенно у недоношенных детей, нередко приводит к тяжёлым последствиям. В 55% случаев внутричерепные кровоизлияния сопровождаются психоневрологическими нарушениями, а у 30% новорожденных развиваются инвалидизирующие состояния, такие как центральные параличи и ментальные расстройства [6].
Диагностика геморрагической болезни новорожденных (ГБН) основывается на совокупности анамнестических данных, клинической картины и результатов лабораторных исследований. Современные методы позволяют не только выявить заболевание, но и определить степень его тяжести, а также возможные осложнения.
При сборе анамнеза учитываются факторы риска, такие как прием матерью во время беременности лекарственных препаратов (антикоагулянты, антибиотики, противосудорожные средства), наличие гестоза, преэклампсии или заболеваний печени. У ребёнка важны данные о характере вскармливания (грудное вскармливание без профилактики витамином K), перенесённые внутриутробные патологии и осложнения в родах [3].
Клиническая картина, как правило, проявляется кровотечениями различной локализации: из пупочной культи, ЖКТ, носа, кожи и внутренних органов. Особое внимание уделяется состояниям, требующим неотложной помощи, таким как внутричерепные кровоизлияния и массивные кровопотери [2].
Основой лабораторной диагностики ГБН является коагулограмма, позволяющая выявить характерные изменения свертывающей системы крови:
— Удлинение активированного частичного тромбопластинового времени (АЧТВ), указывающее на гипокоагуляцию по внутреннему пути свертывания.
— Удлинение протромбинового времени, отражающее гипокоагуляцию по внешнему пути.
— Снижение протромбина по Квику до уровня менее 60%.
При этом уровни фибриногена, фактора Виллебранда и тромбоцитов остаются в пределах нормы, что позволяет дифференцировать ГБН от других нарушений гемостаза [2].
Современные генетические исследования также играют важную роль. Полиморфизмы гена VKORC1, кодирующего 1-эпоксидредуктазу витамина K, ассоциируются с повышенным риском внутрижелудочковых кровоизлияний у новорожденных. Носители аллеля 1639A этого гена имеют сниженный уровень витамина K, что подтверждено логистическим регрессионным анализом. VKORC1 регулирует связывание витамина K1 в его эпоксидной и хиноновой формах, влияя на концентрацию активного витамина K в организме [6].
Инструментальные методы исследования позволяют оценить степень повреждения внутренних органов, особенно головного мозга.
Нейросонография помогает выявить анте-, интра- и постнатальные факторы риска внутрижелудочковых кровоизлияний, уточнить время их возникновения и степень поражения мозговой ткани.
Магнитно-резонансная томография (МРТ) обеспечивает детализированное изображение топографии и размеров кровоизлияний, а также позволяет диагностировать сопутствующие изменения в мозговой ткани и ассоциированные кровоизлияния в мозжечке [21].
При постановке диагноза ГБН важно исключить другие заболевания, сопровождающиеся геморрагическим синдромом и нарушениями системы свертывания крови. Дифференциальный диагноз проводится с наследственными коагулопатиями (например, гемофилией), тромбоцитопениями, синдромом диссеминированного внутрисосудистого свертывания (ДВС), а также синдромом проглоченной крови.
Необходимо учитывать и травматические повреждения, патологии сосудов и другие сопутствующие нарушения со стороны ЖКТ, такие как ангиоматоз кишечника или папилломы ЖКТ, которые могут проявляться сходной клинической симптоматикой [4].
Лечение геморрагической болезни новорожденных (ГБН) направлено на устранение дефицита витамина K, коррекцию нарушений свертываемости крови и ликвидацию последствий кровотечений. Основу терапии составляет фармакологическое, трансфузионное и при необходимости хирургическое вмешательство.
Основным методом лечения ГБН является незамедлительное введение витамина K. В России препаратом выбора выступает менадион натрия бисульфат (Викасол), представляющий собой синтетический аналог витамина K. Его действие начинается через 8–24 часа после введения. Однако зарубежные специалисты предпочитают использовать препараты натурального витамина K1, такие как Конакион и Канавит (фитоменадион), которые оказывают эффект уже через 2 часа. Преимущество натуральных форм заключается в их более быстром действии и меньшем риске побочных эффектов [5].
При выраженных кровотечениях, сопровождающихся значительной кровопотерей, необходима коррекция нарушений гемостаза с использованием:
— Свежезамороженной плазмы для восполнения дефицита факторов свертывания.
— Концентрированного протромбинового комплекса, который содержит витамин K-зависимые факторы свертывания и позволяет быстро восстановить свертывающую способность крови [3].
Для новорожденных с желудочно-кишечными кровотечениями применяется специальная гемостатическая смесь, включающая:
— 50 мл 5% раствора эпсилон-аминокапроновой кислоты,
— 1 мл 12,5% раствора этамзилата натрия,
— флакон (или ампулу) сухого тромбина.
Эта смесь вводится через зонд в желудок ребенка по 5 мл три раза в сутки, что способствует остановке кровотечения и уменьшению его интенсивности.
При тяжелых внутричерепных кровоизлияниях, угрожающих жизни ребенка, может потребоваться хирургическое вмешательство. Перед операцией проводится коррекция показателей свертываемости крови (протромбиновое время, тромбиновая активность, международное нормализованное отношение).
Современные подходы к хирургическому лечению включают минимально инвазивные методы. В частности, в больнице Национального университета Тайваня применяют минимально инвазивную нейрохирургию для лечения внутричерепных кровоизлияний, связанных с коагулопатией. Метод включает эндоскопическую аспирацию сгустков крови, с использованием тромболитиков или без них. Этот подход обеспечивает быстрое восстановление, сокращает период интенсивной терапии и снижает риск повторных кровоизлияний и неврологических осложнений. В сравнении с краниотомией, минимально инвазивные методы оказываются менее травматичными и более эффективными [2].
Профилактика геморрагической болезни новорожденных (ГБН) базируется на восполнении дефицита витамина K, который имеется у всех новорожденных. Уровень витамина K в пуповинной крови часто ниже порога обнаружения, составляя всего 0,02 нг/мл, что указывает на физиологическую недостаточность данного витамина у младенцев. Это обусловлено ограниченной транспортировкой витамина через плаценту, низким его содержанием в грудном молоке и отсутствием синтеза в кишечнике из-за стерильности микрофлоры у новорожденного.
Наиболее эффективным методом профилактики считается парентеральное введение витамина K в первые часы после рождения. Внутримышечное введение обеспечивает быстрое и длительное поддержание уровня витамина K, что подтверждено многочисленными исследованиями [24]. В России рекомендовано применение 1%-го раствора менадион натрия бисульфита (Викасола) в дозе 1,0–1,5 мг/кг/сут, но не более 4 мг в сутки. Этот подход снижает риск развития всех форм ГБН, включая позднюю [4].
Международные протоколы, такие как рекомендации Американской академии педиатрии, предусматривают введение от 0,5 мг до 1 мг витамина K в зависимости от массы тела новорожденного. Аналогичные схемы применяются в Австралии, Германии, Нидерландах и других странах [7].
Альтернативой внутримышечному введению может быть пероральный приём витамина K, особенно в случаях, когда родители отказываются от инъекций. Например, Канадское педиатрическое общество рекомендует следующую схему: 2 мг витамина K в первые 6 часов после рождения, с повторными дозами в 2–4 недели и 6–8 недель жизни. В Швейцарии также применяются схемы перорального приёма: 2 мг при рождении, затем по 1–2 мг еженедельно в течение первых трёх месяцев у детей на грудном вскармливании [2].
Однако эффективность перорального пути зависит от соблюдения режима приёма. Исследования показывают, что пероральная профилактика менее надёжна, особенно у младенцев с нарушением всасывания витамина K из-за холестаза, атрезии желчевыводящих путей или других заболеваний.
Недоношенные новорождённые составляют особую группу риска из-за незрелости их систем гемостаза. Для таких детей рекомендуется более интенсивный мониторинг и применение профилактических мер, включая введение препаратов крови (тромбоцитов, свежезамороженной плазмы) даже при отсутствии кровотечений. Этот подход снижает риск развития геморрагического синдрома.
Несмотря на доказанную пользу витамина K, необходимо соблюдать строгую дозировку. В литературе описаны случаи передозировки при чрезмерном применении менадиона (синтетического водорастворимого аналога витамина K), которые привели к развитию гемолитической анемии, гипербилирубинемии и билирубиновой энцефалопатии у детей первого года жизни [3].
Профилактика ГБН, включающая введение витамина K, является основой предотвращения как ранних, так и поздних форм заболевания. Внутримышечное введение остаётся золотым стандартом, но использование пероральных схем возможно при соблюдении строгого протокола. Особое внимание следует уделять недоношенным детям, которые наиболее уязвимы к развитию коагулопатий. Грамотное применение профилактических мер, соответствующих клиническим рекомендациям, минимизирует риски и обеспечивает здоровое развитие новорожденных.
Таким образом, внедрение более универсальных и доступных профилактических мероприятий позволит снизить заболеваемость и улучшить прогноз для новорожденных, а также сократить риск тяжёлых осложнений, связанных с геморрагической болезнью.
Список литературы
- Закирова B., Хусаинова С. и Очилова B. «Состояние неврологических симптомов у новорожденных с геморрагической болезнью». Международный журнал научной педиатрии, т. 2, вып. 3, март 2023 г., сс. 88-91, doi:10.56121/2181-2926-2023-2-3-88-91.
- Zakirova B. I., Khusainova Sh. K., Ochilova B.S. Journal of Hepato-Gastroenterological Research. 2022;3:45–8. https://doi.org/10.26739/2181-1008.
- R.F. Tepaev, O.B. Gordeeva , V.V. Botvinyeva , O.K. Botvinyev. Hemorrhagic syndrome in infants. Pediatric Pharmacology 2015;12:310–4.
- Иванов Д. О. История изучения геморрагической болезни новорожденных. Педиатр. 2017; 4 (8): 118-125. DOI: 10.17816/PED84118-125.
- Саркисян Е. А., Левченко Л. А, Фёдорова Т. В. Поздняя геморрагическая болезнь у новорожденного. Описание клинического наблюдения. Quantum Satis. 2020; 1-4 (3): 37-40
- Бражникова О. В., Заплатников А. Л., Никитин В. В. и др. Актуальная проблема Витамин К-дефицитная коагулопатия у детей первых месяцев жизни: решенные вопросы и актуальные проблемы. РМЖ. 2018; 2 (ll): 75-78. Сарыева О. П., Проценко Е. В., Кулида Л. В. Внутрижелудочковые кровоизлияния у глубоконедоношенных новорожденных: предикторы развития. Российский вестник перинатологии и педиатрии. 2022; 67 (3): 11-17. DOI: 10.21508/1027-4065-2022-67-3-11-17.
- Киселева Л. Г., Чумакова Г. Н., Соловьев А. Г., Харькова О. А., Косяков Д. С., Ульяновский Н. В., Грызунова Е. М. Содержание витамина LECHASCHI VRACH, VOL. 26, № 9, 2023, https://journal.lvrach.ru/ 63 Pediatry. Neonatology К1 в пуповинной крови новорожденных г. Архангельска. Российский вестник перинатологии и педиатрии. 2017; 62 (2): 49-53. DOI: 10.21508/1027-4065-2017-62-2-49-53